清滤率(Clearance rate,CR)是指单位时间内水生生物摄食水中颗粒饵料时滤过的水的体积。它不仅直接反映了生物的摄食情况,而且也是一个重要的反映生物自身生理状态的指标。因此,双壳类清滤率的改变可以在一定程度上反映出污染物的影响程度[1]。
链状裸甲藻(Gymnodinium catenatum)是高毒性甲藻,可产生麻痹性贝类毒素(Paralytic shellfish toxins,PST),也是中国沿海常见的赤潮藻种之一,在中国许多海区曾检测到其游动细胞和孢囊,并在局部海域形成赤潮[2]。2017年6月,福建省漳州、泉州海域曾发生链状裸甲藻赤潮,造成了赤潮海域的贻贝、牡蛎、扇贝等滤食性贝类体内PST含量超标,并导致多地民众因食用翡翠贻贝(Perna viridis)而中毒的事件发生[3]。已有研究表明,产毒藻能够对贝类产生影响,如塔玛亚历山大藻(Alexandrium tamarense)会抑制紫贻贝(Mytilus edulis)的清滤率[1];微小亚历山大藻(Alexandrium minutum)会影响菲律宾蛤仔(Ruditapes philippinesis)的生理状态,高密度产毒藻对贝类会有一定的摄食抑制[4]。关于链状裸甲藻对滤食性贝类的影响报道较少。
暴露于产毒藻中的贝类的清滤率的变化可以直接反映出其对毒素的敏感性,并能够指示随后的毒素累积情况[5]。本文以链状裸甲藻为产毒藻,以沿岸海域常见无毒硅藻中肋骨条藻(Skeletonema costatum)为对照,研究链状裸甲藻对翡翠贻贝清滤率的影响,为研究PST在滤食性贝类体内的累积规律、贝类脱毒与净化提供基础资料。
1 材料与方法
1.1 受试生物
试验用链状裸甲藻和中肋骨条藻藻液均由厦门大学海洋微型生物保种中心提供,链状裸甲藻藻种于2017年6月分离自泉州海域。翡翠贻贝来自漳州东山乌礁湾海域,选择活力好、健康、无外伤的翡翠贻贝运送至福建省水产研究所生态试验场。将翡翠贻贝置于25 L玻璃水槽中,按2 ind/L的试验密度进行驯养。驯养3 d,期间每日定时换水,并投喂中肋骨条藻(水体中藻液初始密度为5.0×106 cells/L)2次,全天充气。驯养期间翡翠贻贝活力良好、摄食正常,死亡率为0.3%。试验前随机抽取30只翡翠贻贝进行生物性状测量,其壳宽为(7.0±0.3)cm、壳长为(3.2±0.1)cm、全重为(25.1±2.7)g。
1.2 试验方法与条件
试验所用海水来自厦门海域。试验期间海水盐度为(30.0±0.1),水温为(23±1) ℃,pH为8.00~8.12,溶解氧浓度为7.19~7.38 mg/L。
1.2.1 1 h清滤率试验
根据预试验结果,试验组和对照组分别设6个试验梯度,试验组(G1~G6组)采用链状裸甲藻投喂翡翠贻贝,藻液密度分别为2.5×104、5.0×104、1.0×105、2.5×105、5.0×105和1.0×106 cells/L;对照组(S1~S6组)采用中肋骨条藻投喂翡翠贻贝,藻液密度分别为1.0×105、2.5×105、5.0×105、1.0×106、2.5×106和5.0×106 cells/L;各组均设3个平行。将大小一致、健康的翡翠贻贝放入3 L玻璃烧杯内,每个烧杯盛3只翡翠贻贝、1.5 L藻液,微充气,1 h后取海水和翡翠贻贝样品。海水样品取样1 L,用鲁哥氏液固定,在实验室静置24 h后浓缩、计数,用于检测藻液密度,计算单个翡翠贻贝的清滤率。取出各组翡翠贻贝的贝肉,置于105 ℃烘箱内烘干4 h后称重,用于换算翡翠贻贝单位干重的清滤率。
单位个体清滤率(CRind)计算公式采用Coughlan J(1969)提出的公式[6]:
由于翡翠贻贝的个体大小存在差异,本文测定了试验组和对照组翡翠贻贝的软体部干重,参考杨晓新等[7]文献计算公式,换算为单位干重清滤率(CRmass)。
式(1)和(2)中:V为试验水体的体积(L);C0、Ct为试验开始和试验t时间的藻细胞密度(cells/L);n为试验翡翠贻贝个数(ind);W为试验翡翠贻贝软体部干重(g);t为试验时间(h)。
1 h清滤率试验分别采用公式(1)和(2)进行计算;长期清滤率试验由于无法准确获得每批次翡翠贻贝样品的干重,因此采用公式(1)计算清滤率。
1.2.2 长期清滤率试验
在开展长期清滤率试验前,对翡翠贻贝摄食作用下藻液密度的变化开展预试验,试验周期12 h,以确定投喂藻液频率。根据1 h清滤率试验结果,设置1个试验组和1个对照组,试验组投喂5.0×105cells/L链状裸甲藻,对照组投喂5.0×106cells/L中肋骨条藻,各组均设3个平行。从驯养3 d的翡翠贻贝中,选出大小一致、健康的贻贝置于盛有12 L海水的玻璃水槽中,每组24只贻贝×3个平行,投喂后分别于0.5、1、2、4、6、8、10、12 h取适量海水样品用于藻细胞计数。
根据预试验结果开展翡翠贻贝摄食链状裸甲藻的累积试验(10 d)和排出试验(28 d),同步进行清滤率试验,试验周期为38 d。试验设置1个试验组和1个对照组,试验组投喂5.0×105cells/L链状裸甲藻,对照组投喂5.0×106cells/L中肋骨条藻,各组均设3个平行。从驯养3 d的翡翠贻贝中,选出大小一致、健康的贻贝,每组40只贻贝×3个平行,分别置于盛有20 L海水的玻璃水槽中。每日上午定时换水1次,定时投喂藻液2次(08:00和20:00)。试验开始后分别在累积1、2、4、6、8和10 d的09:00(投喂藻液后1 h),试验组和对照组各取海水样品100 mL用于藻细胞计数。累积试验结束后,试验组改投喂中肋骨条藻(试验密度5.0×106cells/L),开始排出试验。每隔4 d的09:00(投喂藻液后1 h),试验组和对照组各取海水样品100 mL进行藻细胞计数,并计算翡翠贻贝的清滤率。
1.3 数据处理
应用SPSS 23软件对试验数据进行单因素方差分析和T检验,P<0.05表示差异显著。
2 结果与分析
2.1 1 h清滤率试验中翡翠贻贝清滤率的变化
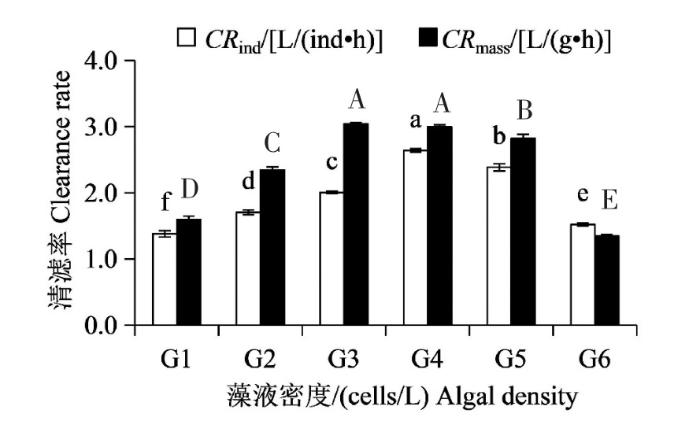
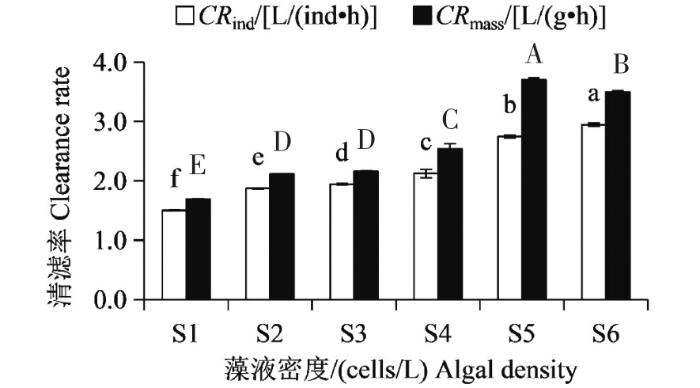
当链状裸甲藻密度在2.5×104~1.0×106 cells/L之间时,翡翠贻贝单位个体清滤率的波动范围在(1.38±0.05)~(2.64±0.03)L/(ind·h)之间,呈先升高后降低的趋势,不同密度组之间清滤率差异显著(P<0.05)(图1)。当藻液密度为2.5×104 cells/L时,翡翠贻贝清滤率最小。随着藻液密度的增大,翡翠贻贝清滤率逐渐升高,当藻液密度升高至2.5×105 cells/L,达到赤潮基准密度时(链状裸甲藻体长48~65 μm,根据HY/T 069—2005《海洋赤潮监测技术规程》,对应的赤潮基准密度为>2×105 cells/L)[8],翡翠贻贝清滤率最大,为(2.64±0.03)L/(ind·h)。随着藻液密度的继续升高,翡翠贻贝清滤率显著下降(P<0.05),5.0×105cells/L试验组和1.0×106cells/L试验组清滤率分别为(2.38±0.06)、(1.52±0.02)L/(ind·h)。对照组随着中肋骨条藻密度从1.0×105 cells/L逐渐增加至5.0×106 cells/L,翡翠贻贝单位个体清滤率呈逐渐升高的趋势,从(1.50±0.01)L/(ind·h)升高至(2.95±0.02)L/(ind·h),不同密度组之间清滤率差异显著(P<0.05)(图2)。
图1
图1
1 h清滤率试验中试验组清滤率的变化
注:G1~G6链状裸甲藻藻液密度分别为2.5×104、5.0×104、1.0×105、2.5×105、5.0×105、1.0×106 cells/L。同一单位下,不同字母表示清滤率差异显著(P<0.05),相同则差异不显著(P>0.05)。下同。
Fig.1
The change of clearance rate of the experimental group in the 1 h clearance rate experiment
Notes: The algal density of G.catenatum were 2.5×104, 5.0×104, 1.0×105, 2.5×105, 5.0×105, 1.0×106 cells/L, respectively. Under the same unit,the different letters in the figure indicated that there was a significant difference in the clearance rate(P<0.05),or the same letters meant no difference(P>0.05).The same as below.
图2
图2
1 h清滤率试验中对照组清滤率的变化
注:S1~S6中肋骨条藻藻液密度分别为1.0×105、2.5×105、5.0×105、1.0×106、2.5×106和5.0×106 cells/L。
Fig.2
The change of clearance rate of the control group in the 1 h clearance rate experiment
Notes:The algal density of S.costatum were 1.0×105, 2.5×105, 5.0×105, 1.0×106 ,2.5×106, 5.0×106 cells/L, respectively.
试验组翡翠贻贝单位干重清滤率的波动范围在(1.35±0.02)~(3.04±0.02)L/(g·h)之间,与单位个体清滤率变化趋势基本一致,呈先升高后降低的趋势(图1),但是清滤率最高值和最低值所对应的链状裸甲藻密度不一致。当链状裸甲藻密度为2.5×104 cells/L时,翡翠贻贝清滤率为(1.59±0.05)L/(g·h)。随着藻液密度的增大,翡翠贻贝清滤率逐渐升高,当藻液密度升高至1.0×105cells/L,接近赤潮基准密度时,翡翠贻贝清滤率最大,为(3.04±0.02)L/(g·h)。当藻液密度升高至2.5×105 cells/L时,翡翠贻贝清滤率为(3.00±0.03)L/(g·h),与1.0×105 cells/L试验组相比差异不显著(P>0.05)。随着藻液密度的继续升高,翡翠贻贝清滤率显著下降(P<0.05),5.0×105 cells/L试验组清滤率为(2.82±0.07)L/(g·h);1.0×106 cells/L试验组清滤率最低,为(1.35±0.02)L/(g·h)。对照组翡翠贻贝单位干重清滤率的波动范围在(1.69±0.01)~(3.70±0.03)L/(g·h)之间,呈先升高后降低的趋势(图2)。当中肋骨条藻密度为1.0×105 cells/L时,翡翠贻贝清滤率最低,随着藻液密度的增大,翡翠贻贝清滤率逐渐升高,当藻液密度升高至2.5×106 cells/L,接近赤潮基准密度时(中肋骨条藻体长6~22 μm,对应的赤潮基准密度为>5×106cells/L),翡翠贻贝清滤率最大,为(3.70±0.03)L/(g·h)。当藻液密度继续升高至5.0×106 cells/L时,翡翠贻贝清滤率显著下降(P<0.05),为(3.49±0.03)L/(g·h)。
2.2 长期清滤率试验中翡翠贻贝清滤率的变化
2.2.1 翡翠贻贝滤食作用下藻液密度的变化
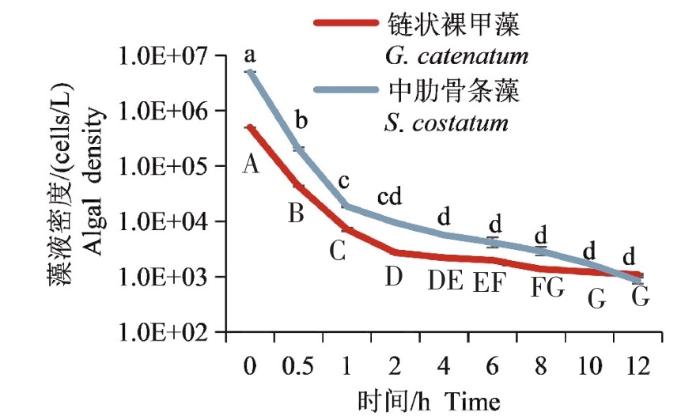
链状裸甲藻和中肋骨条藻的初始密度分别为5.0×105和5.0×106 cells/L,在翡翠贻贝的滤食作用下,藻液密度随着时间的推移逐渐降低。在投喂0.5 h后,链状裸甲藻和中肋骨条藻细胞密度均下降了1个数量级;1 h后下降了2个数量级,但下降的速度有所放缓;12 h后藻液密度均下降至较低的水平,链状裸甲藻和中肋骨条藻的细胞密度分别为1.09×103、8.54×102 cells/L(图3)。根据试验结果,将投喂藻液的频率确定为每隔12 h一次。
图3
图3
翡翠贻贝摄食作用下藻液密度的变化
注:同种藻类下的显著性分析。
Fig.3
The change of algae density under the feeding of P. viridis
Note:Signidicance analysis under the same algae specie.
2.2.2 翡翠贻贝清滤率的变化
累积试验中翡翠贻贝清滤率的变化见图4。试验组投喂5.0×105 cells/L链状裸甲藻,随着累积时间的推移,翡翠贻贝清滤率在(2.09±0.01)~(2.78±0.05)L/(ind·h)范围内上下波动,平均值为2.35 L/(ind·h),累积1 d和10 d的清滤率差异不显著(P>0.05)。对照组投喂5.0×106 cells/L中肋骨条藻,翡翠贻贝清滤率波动范围在(3.09±0.03)~(3.64±0.20)L/(ind·h)之间,平均值为3.31 L/(ind·h),累积1 d和10 d的清滤率差异不显著(P>0.05)。
图4
图4
累积试验中翡翠贻贝清滤率的变化
注:同一组别下的显著性分析。
Fig.4
The change of clearance rate of P. viridis in accumulation experiment
Note:Significance anaylsis under the same group.
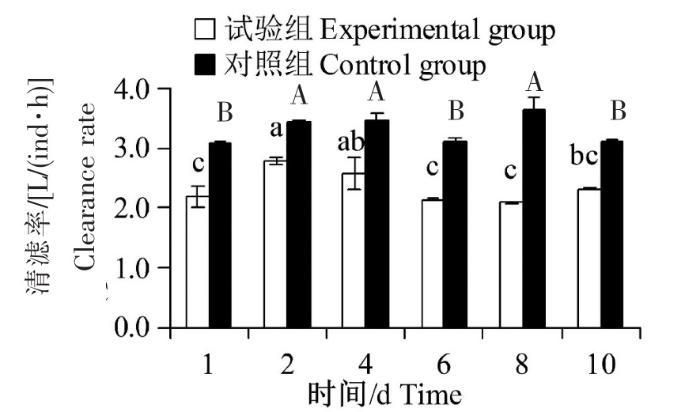
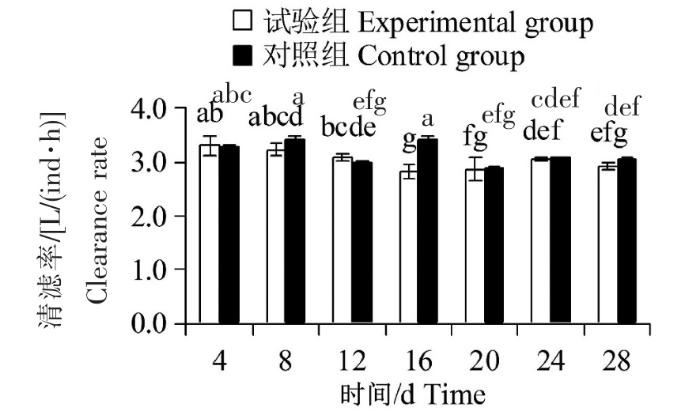
排出试验中,试验组和对照组翡翠贻贝均投喂5.0×106 cells/L中肋骨条藻,其清滤率的变化见图5。试验组和对照组翡翠贻贝清滤率分别在(2.83±0.14)~(3.30±0.17) 和(2.90±0.02)~(3.43±0.06) L/(ind·h)范围内上下波动,平均值分别为3.00、3.14 L/(ind·h),二者无显著差异(P>0.05)。排出28 d与排出4 d相比,试验组和对照组翡翠贻贝清滤率均显著下降(P<0.05),但是与1 h清滤率试验数据相比[5.0×106 cells/L对照组翡翠贻贝的清滤率为(2.95±0.02)L/(ind·h)],排出28 d后翡翠贻贝清滤率变化不显著(P>0.05)。
图5
图5
排出试验中翡翠贻贝清滤率的变化
注:组内、组间的多重比较。
Fig.5
The change of clearance rate of P. viridis in depuration experiment
Note:Multiple comparisons within and between groups.
3 讨论
3.1 贝类摄食率、清滤率的一般变化规律以及摄食率的调节方式
滤食性贝类的取食有两种途径:一是水动力作用,即食物随水流通过主鳃丝直接进入鳃的背缘,随背部纤毛的摆动进入唇瓣;二是黏液纤毛作用,即食物流经鳃的表面,在整个鳃系统的作用下(纤毛摆动、黏液细胞的作用等)进入鳃的腹缘,再沿腹部食物运送沟进入唇瓣[9]。已有研究表明,在适宜的饵料浓度范围内,滤食性贝类的摄食率和清滤率随饵料浓度的增大而升高,呈幂函数关系,这是由于在较高饵料浓度下,过滤同样多的海水得到的饵料增加[10⇓⇓-13]。当超过一定的饵料浓度时,贝类摄食率随饵料浓度的增加而略微降低,清滤率则急剧下降[10⇓⇓-13],这是由于当饵料浓度过高时,双壳贝类食道的食物出现饱和,使其关闭出入水管,限制滤水率[14]。通过降低清滤率来减少滤食的饵料量是滤食性贝类调节摄食率的方式之一,另一种方式是通过排出大量假粪来稳定摄食率。这两种方式在调节贝类摄食率时同时起作用,但是对于不同的饵料质量所起的作用不一样,当饵料中有机物含量较高时,前者起主要作用;当饵料中有机物含量较低时,后者起主要作用[10]。假粪的产生是藻细胞进入贝类鳃后不进入消化道,而是通过简单的黏液包裹后立即从外套膜排出体外。假粪的出现会干扰试验结果的准确性。假粪与真粪的辨别主要依据以下几方面:一是假粪一般呈絮状、片状或团状,而真粪则呈规则的丝状;二是假粪韧性不如真粪,容易破碎;三是假粪产生的时间较真粪早,一般在贝类摄食后10~15 min产生,并且假粪中完整的藻细胞大多数是活细胞[15]。本研究通过预试验,确定了1 h清滤率试验中试验组和对照组藻液密度的设置范围和试验梯度,并开展12 h试验,获得翡翠贻贝摄食作用下藻液密度的变化数据,以确定长期清滤率试验中投喂藻液的密度和频率,避免试验中翡翠贻贝产生假粪。
3.2 翡翠贻贝清滤率“阈值”与藻细胞密度的对应关系
本研究结果表明,翡翠贻贝无论是摄食产毒藻或无毒藻,随着藻液密度的增加,清滤率均呈先升高后降低的变化趋势,与已有的研究结果[10⇓⇓-13]一致。试验组翡翠贻贝单位干重清滤率的峰值出现在链状裸甲藻密度为1.0×105cells/L时,对照组则出现在中肋骨条藻密度为2.5×106 cells/L时,这是由于链状裸甲藻和中肋骨条藻细胞个体大小存在较大差异,因此翡翠贻贝清滤率峰值所对应的藻细胞密度也存在显著差异(P<0.05),但是其有共同规律:两组翡翠贻贝清滤率的峰值均出现在藻细胞密度接近赤潮基准密度时,即当藻细胞密度达到和超过赤潮基准密度时,翡翠贻贝的清滤率均呈下降趋势,说明此时贝类清滤率出现了“阈值”效应,降低了对微藻的滤食能力。解万翠等[16]发现,用微小亚历山大藻投喂近江牡蛎,当藻细胞密度超过1.5×106 cells/L时,牡蛎清滤率显著下降。Murray S A等[17]的研究表明,当微小亚历山大藻密度达到1.0×106 cells/L时,覆瓦珠母贝(Pinctada imbricata)清滤率开始下降,而微小亚历山大藻赤潮基准密度为1×106cells/L。上述研究表明,当藻细胞密度达到或超过赤潮基准密度时,贝类清滤率出现了“阈值”效应,这与本研究结果相似。
赤潮发生时,赤潮生物的大量繁殖会对海洋中其他生物产生危害。不同赤潮生物引发赤潮时的基准密度不同,划分依据为赤潮生物的细胞(个体)大小。本研究贝类清滤率“阈值”效应的出现及其对应的藻细胞大小和密度,也印证了即使是无毒赤潮,在藻细胞密度达到赤潮基准密度后,也会对贝类摄食产生影响。
3.3 链状裸甲藻对翡翠贻贝清滤率的影响
本研究试验组和对照组翡翠贻贝单位干重清滤率的最高值分别为(3.04±0.02)、(3.70±0.03)L/(g·h),与对照组相比,投喂链状裸甲藻的试验组翡翠贻贝的清滤率显著下降(P<0.05),表明链状裸甲藻对翡翠贻贝的摄食产生了影响。其他学者的研究也有类似发现,朱明远等[18]的研究表明,与投喂三角褐指藻(Phaeodactylum tricornutum)相比,投喂亚历山大藻的栉孔扇贝(Chlamys farreri)清滤率显著下降;黄德强等[19]的研究表明,翡翠贻贝对塔玛亚历山大藻的滤食率显著低于扁藻(Platymonas sp.)和三角褐指藻。产毒藻对贝类可能产生行为学和生理学方面的影响,一些贝类可以通过关闭贝壳等减少或避免摄食产毒藻,出现壳瓣闭合、钻沙、清滤率降低等不良反应[5,20 -21],但是这些反应具有种的特异性和地域特异性,不同地域的贝类接触毒藻后会表现出不同的反应[5]。也有一些学者的研究结果不同,Guéguen M等[22]发现,投喂微小亚历山大藻的牡蛎的清滤率无显著性变化,牡蛎对微小亚历山大藻敏感性较低;解万翠等[16]的研究表明,与投喂扁藻相比,投喂微小亚历山大藻的近江牡蛎的清滤率没有降低。以上研究结果表明不同贝类对产毒藻的敏感性存在差异。本研究试验组贻贝清滤率显著下降(P<0.05),但其没有出现壳瓣闭合等明显不适反应,总体而言贻贝对链状裸甲藻的敏感性不高。以往研究[23-24]认为,对产毒藻敏感性较低的贝类体内累积的PST含量较高,而对毒素敏感性较高的贝类累积的PST含量较低。项目组2017年6月对链状裸甲藻赤潮海域贝类的跟踪监测结果显示,与牡蛎、蛤类、扇贝等滤食性贝类相比,翡翠贻贝体内PST含量最高,说明与其他贝类相比,其对PST具有更高的累积能力,De Carvalhe I L等[25]的研究结果也证实了这一点。
长期累积试验期间翡翠贻贝的清滤率在一定的范围内上下波动,累积1 d和10 d的清滤率差异不显著(P>0.05);排出试验期间翡翠贻贝清滤率同样呈上下波动之势,与1 h清滤率试验数据相比,排出28 d后其清滤率的变化不显著(P>0.05),且试验组和对照组贻贝清滤率无显著差异(P>0.05)。推测长期累积和排出试验中翡翠贻贝清滤率的上下波动是由其个体大小的差异造成的。在长期摄食链状裸甲藻的过程中,翡翠贻贝对产毒藻有一定的适应性,与短期滤食相比清滤率无显著变化(P>0.05)。解万翠等[16]的研究表明,长期(5 d)滤食微小亚历山大藻的近江牡蛎的清滤率没有发生显著变化,这与本研究结果一致。
付家想等[26]、蓝文陆等[27-28]研究认为,不同种类饵料对香港巨牡蛎(Crassostrea hongkongensis)的清滤率和摄食率有着显著的影响,主要影响因素为藻细胞大小、形状、营养质量和密度等。朱雨瑞等[29]发现,稚贝优先滤食饵料效果好的微藻,对饵料效果差的微藻摄食速度最慢。本试验材料翡翠贻贝属于成贝,对链状裸甲藻和中肋骨条藻的摄食不存在受贝类口径影响的问题。中肋骨条藻为硅藻,具有不易变形的硅酸盐外壳,更容易被滤食性贝类的鳃保留,与甲藻相比更适合滤食性贝类摄食[30-31]。在整个试验过程中,翡翠贻贝无行为方面的不适反应,长期滤食链状裸甲藻后的清滤率的变化也不显著。综上,试验组贻贝清滤率显著下降的原因可能是综合藻细胞大小、外部构造、饵料密度、营养质量、PST毒性等因素差异造成的结果。
4 结论
通过研究链状裸甲藻对翡翠贻贝清滤率的影响,得出如下结论:
1)翡翠贻贝无论是摄食产毒藻或无毒藻,随着藻细胞密度的升高,清滤率的变化均呈先升高后降低的趋势,峰值出现在藻细胞密度接近赤潮基准密度时。
2)试验组和对照组翡翠贻贝清滤率的最高值分别为(3.04±0.02)、(3.70±0.03)L/(g·h),试验组翡翠贻贝的清滤率显著下降(P<0.05),表明链状裸甲藻对翡翠贻贝的摄食产生了影响,可能是由藻细胞大小、外部构造、饵料密度、营养质量、PST毒性等因素差异造成的。
3)长期滤食链状裸甲藻的翡翠贻贝的清滤率基本保持在初始水平,与短期滤食相比无显著变化(P>0.05)。
参考文献
有毒亚历山大藻(Alexandrium spp.)和链状裸甲藻(Gymnodinium catenatum)孢囊在中国沿海的分布
[J].
2017年福建海域链状裸甲藻赤潮事件应急处置与思考
[J].福建是我国赤潮多发省份之一,2000—2017年共发现赤潮219起,其中35起赤潮造成养殖损失或群众健康受损事件。做好有毒赤潮应急处置,对保障人民群众生命安全,维护海洋渔业经济健康发展,服务福建生态省建设至关重要。本文以2017年福建中南部沿海海域链状裸甲藻赤潮事件为例,对赤潮事件过程、主要应急处置措施、存在的问题进行分析与讨论。在此次有毒赤潮事件处置过程中,政府部门采取及时控制贝毒超标水产品养殖区源头、根据赤潮动态调整监视监测工作、主动公开赤潮有关情况、适时终止应急响应等措施,有效地遏制赤潮对社会和水产品质量安全等不利影响的进一步扩大,切实保障群众水产品食用安全及生命财产的安全。针对事件过程中暴露出部门联动、赤潮监测能力等方面的不足,提出完善协同应急响应机制、加强地市级基本应急能力建设、利用新技术开展有毒赤潮生物监测、推广快检技术以加强海水贝类质量安全监测等建议。
The effects of the toxic dinoflagellate Protogonyaulax tamarensis on the feeding and behaviour of bivalve molluscs
[J].
The estimation of filtering rate from the clearance of suspensions
[J].
Mecharusms of suspension feeding in bivalves: resolution of current controversies by means of endoscopy
[J].Controversy concerning the mechanism of suspension feeding in bivalves centers around whether particle capture and transport on the gills (ctenidia) is accomplished via mucociliary or hydrodynamic action. Evidence for and against these fundamentally different processes has been based on examinations of isolated feeding structures and dissected specimens, techniques that may produce artifactual data owing to the trauma associated with the procedures. In the present study, in vivo observations of the ctenidia of undisturbed bivalves, made with a fiber‐optic endoscope and video image‐analysis system, revealed that the two mechanisms are not mutually exclusive. Both mucociliary and hydrodynamic mechanisms function concurrently at different sites on the ctenidia, thereby minimizing particle loss and optimizing particle transport efficiency. The importance of mucus in the normal feeding process of bivalves is confirmed. These findings refute results of previous studies that used surgically invasive techniques and emphasize the importance of making observations on morphologically intact specimens.
Differential accumulation of paralytic shellfish toxins from Alexandrium minutum in the pearl oyster, Pinctada imbricata
[J].
Detoxificationof Pacific oyster Crassostrea gigas fedondiets of Skeletonema costatum with and without silt, following PSP contamination by Alexandrium minutum
[J].
Uptake kinetics of paralytic shellfish toxins from the dinoflagellate Alexandrium fundyense in the mussel Mytilus edulis
[J].
Effectsof short-term exposure to paralytic shellfish toxins on clearance rates and toxin uptake in five species of New Zealand bivalve
[J].Algal blooms produced by toxic dinoflagellates have increased worldwide, resulting in economic losses to aquaculture and fisheries. Bivalve species differ in their ability to feed on toxin-producing dinoflagellates and this could result in differences in toxin accumulation among species. In New Zealand, the effects of paralytic shellfish poisoning (PSP) toxins on the physiology of bivalve molluscs are relatively unknown. We hypothesised that the feeding responses of five New Zealand bivalve species exposed to PSP-toxic dinoflagellates would be species-specific, affecting their accumulation of toxins. Each species was exposed to toxic and non-toxic species of Alexandrium spp. and clearance rate used as an index of sensitivity to PSP toxins. Clearance rates for the mussel Perna canaliculus and the clam Dosinia anus were unaffected by the presence of toxic dinoflagellates, whereas the rate in the scallop Pecten novaezelandiae decreased significantly. There were variable results for the clam Paphies donacina and the oyster Ostrea chilensis. Species-specific biotransformation of PSP-toxins had taken place in the bivalve tissues. We conclude that the rate of accumulation of PSP toxins in the tissues of the bivalve species was influenced by their feeding behaviour and the different chemical processes that had taken place in their tissues.
Paralytic shellfish poisoning due to ingestion of contaminated mussels: a 2018 case report in Caparica (Portugal)
[J].
Phytoplankton community structure defined by key environmental variables in Tagus estuary, Portugal
[J].In this work, we analyze environmental (physical and chemical) and biological (phytoplankton) data obtained along Tagus estuary during three surveys, carried out in productive period (May/June/July) at ebb tide. The main objective of this study was to identify the key environmental factors affecting phytoplankton structure in the estuary. BIOENV analysis revealed that, in study period, temperature, salinity, silicate and total phosphorus were the variables that best explained the phytoplankton spatial pattern in the estuary (Spearman correlation, rho=0.803). A generalized linear model (GLM) also identified salinity, silicate and phosphate as having a high explanatory power (63%) of phytoplankton abundance. These selected nutrients appear to be consistent with the requirements of the dominant phytoplankton group, Baccilariophyceae. Apparently, phytoplankton community is adapted to fluctuations in light intensity, as suspended particulate matter did not come out as a key factor in shaping phytoplankton structure along Tagus estuary.